Procalcitonin
این تست به چه نامهای دیگری شناخته میشود؟
برای تغییر این متن بر روی دکمه ویرایش کلیک کنید. لورم ایپسوم متن ساختگی با تولید سادگی نامفهوم از صنعت چاپ و با استفاده از طراحان گرافیک است.
هدف از انجام تست چیست؟
سپسیس یک پاسخ التهابی سیستمی به عفونت است،که بسیار جدی و تهدید کننده بالقوه حیات است.تشخیص سپسیس به وسیله مستندات بالینی ( مثل نتیجه آزمایش کشت باکتریایی) و وجود 2 علامت از 4علائم زیر است:
1-تب بالای 38 درجه سلسیوس یا دمای بدن کمتر از 36 درجه سلسیوس
2-ضربان قلب بیشتر از 90
3-افزایش تهویه (تنفس) به بیشتر از 20
4-شمارش گلبول های سفید بیشتر از و یا کمتر از
پروکلسیتونین، پیش ساز هورمون کلسیتونین است که توسط سلول های C تیروئید ساخته می شوند.در سندروم پاسخ التهابی سیستمیک، توکسین های میکروبی و واسطه های پروتئینی التهابی مثل سایتوکاین ها،اینترلوکین 1، پروستاگلاندین ها و فاکتور فعال کننده پلاکتی ممکن است باعث افزایش تولید پروکلسی تونین از سلول های غیرتیروئیدی و غیرنورواندوکرینی شود.هرفاز از پاسخ التهابی ،مجموعه ای از اتفاقات دیگری را رقم می زند که ممکن است به شوک سپتیک و مرگ ختم شود.
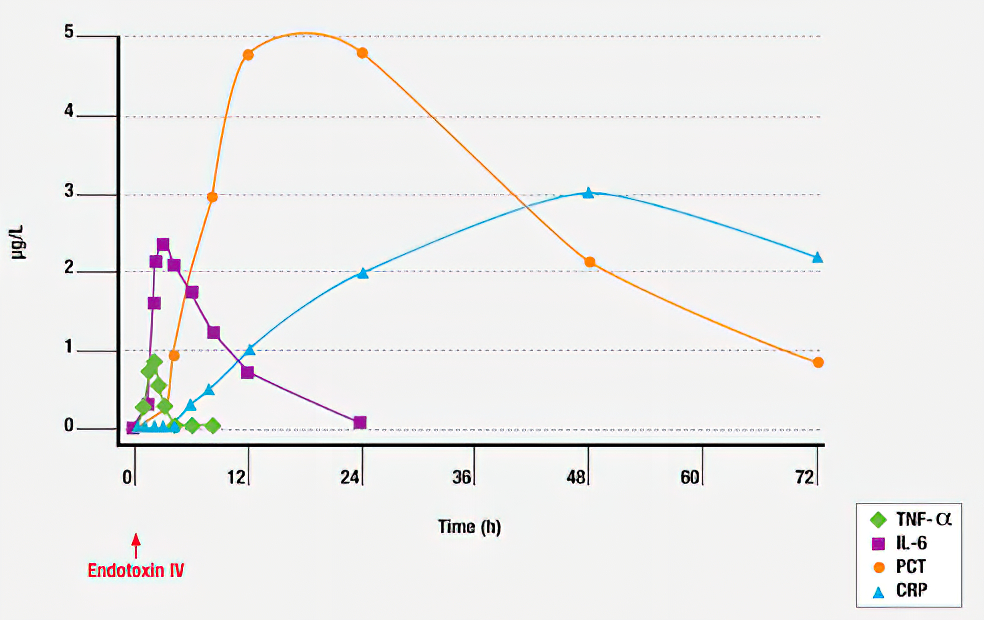
پروکلسی تونین پس از 2 تا 4 ساعت از شروع پاسخ التهابی قابل تشخیص بوده و در مدت 12 تا 24 ساعت به نقطه اوج خود می رسد.اندازه گیری های متوالی برای نظارت بر ریسک پیشرفت سپسیس و یا پاسخ به درمان، می تواند مفید باشد.
این تست چه زمانی درخواست میشود؟
- کمک به تشخیص آلودگی خون با باکتری(سپتیسمی)
- برای کمک به تشخیص عفونت باکتریایی و ریسک پیشرفت سپسیس
- کمک به افتراق عفونت باکتریایی و مننژیت ویروسی(نوعی مننژیت ناشی از عفونت ویروسی است که منجر به التهاب مننژها (غشاهای پوشاننده مغز و نخاع) می شود.)
- پایش پاسخ به درمان با آنتی بیوتیک
ارتباط تست پروکلسیتونین با بیماری کووید-19
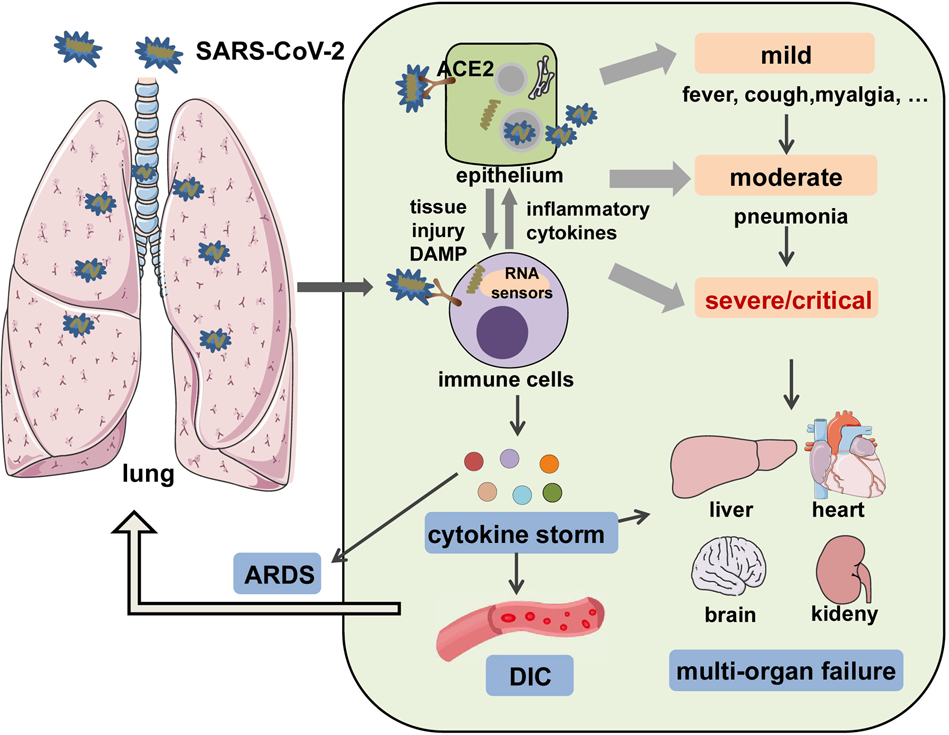
بیماران مبتلا به COVID-19 که در حالت شدید بیماری قرار دارند،اغلب دارای سطوح بالایی از عوامل التهابی در سرم هستند. طوفان التهابی سایتوکاین نقش مهمی در پیشرفت بیماری، این بیماران دارد. ایجاد پاسخ ایمنی بیش از حد باعث ایجاد طوفان سایتوکاین می شود ، که مجموعه ای از اثرات بد را بر بدن ایجاد می کند.سنجش شاخص های التهابی ، مانند پروکلسیتونین ، پروتئین واکنشی C و اینترلوکین 6، ممکن است اهداف بالقوه ای برای درمان COVID-19 باشند. پروکلسیتونین یک نشانگر فعالیت التهابی سیستمیک، در مراحل اولیه پس از عفونت ناشی از محرکهای التهابی است،که با پیش آگهی بیماریهای عفونی در ارتباط است.سطوح خونی پروکلسیتونین با شدت بیماری COVID-19 در ارتباط است ، اما برخی از عوامل می توانند در انجام آزمایش و تفسیر نتایج تداخل ایجاد کنند.به عنوان مثال: در مطالعه ای که بر روی بیماران دیابتی انجام شد، ارتباط مثبت بین PCT و شدت COVID-19 کاهش یافت.
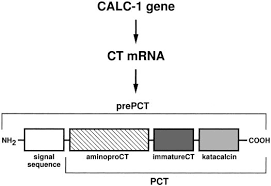
طی مطالعات مختلف، محققین گزارش داده اند، بیماران شدید و بحرانی COVID-19 ممکن است سرکوب ایمنی نسبتاً قابل توجهی را از خود نشان دهند.همچنین بیشتر بیماران مبتلا به COVID-19 که در حالت شدید بیماری قرار دارند و یا فوت شده اند، به عفونت همزمان یا نارسایی چند عضو مبتلا بودند. در عفونت های شدید (باکتریایی ،قارچی و انگلی) ، سپسیس و نارسایی چند ارگان ، سطح PCT در سرم افزایش می یابد. این عفونت ها باعث بیان ژن Calc-I می شود(که PCT را کد می کند)و منجر به انتشار گسترده PCT درخون می شود. افزایش سطح PCT سرم ،در بیماران مبتلا به عفونت ریوی نیزگزارش شده است که این اتفاق، نظر فوق را تأیید می کند.
جدیدترین تحقیقات نشان می دهند که عفونت شدید ویروسی-تنفسی در غیاب پنومونی باکتریایی باعث افزایش سطح سرمی پروکلسیتونین می شود.این بازخورد مثبت بین پروکلسیتونین و سایتوکاین های پیش التهابی متعاقباً منجر به یک واکنش التهابی شدید سیستمیک می شود و یافته های اخیر نشان می دهد که بیماران مبتلا به COVID-19 با PCT بالا،در معرض خطر بیشتری هستند.
جمع بندی تحقیقات انجام شده در این موضوع، نشان می دهد که میانگین سطح سرمی PCT بیمارانی در حالت شدید بیماری قرار دارند می تواند تا چهار برابر بیماران در حالت متوسط و تقریباً هشت برابر بیشتر در بیماران بحرانی افزایش یابد. به نظر می رسد سطح PCT وابسته به شدت بیماری است و با عفونت همزمان باکتریایی می تواند مرتبط باشد ، زیرا میزان عفونت با میزان افزایش سطح PCT در بیماران در ارتباط است. علاوه بر این ، افزایش تدریجی سطوح PCT ممکن است پیش آگهی بدتری را در مورد وخیمتر شدن شرایط بیمار را پیش بینی کند.
چه نوع نمونهای برای این تست نیاز است؟
برای این آزمایش، خونگیری از ورید بازویی انجام می شود.
مراجعه کننده قبل از انجام آزمایش باید چه شرایطی را رعایت کند؟
نیاز به رعایت شرایط خاصی نیست.
دامنه مرجع:
در آزمایشگاه وحید مقادیر طبیعی به صورت زیر گزارش می شود:
No Bacterial Infection: < 0.3
Local Bacterial Infection: 0.3 – 0.5
Systemic Infection(Sepsis): 0.5 – 2
Severe Sepsis: 2 – 10
تفسیر نتایج
پروکلسیتونین در شرایط زیر افزایش می یابد:
سپتیسمی
جراحی های سنگین
اختلال در عملکرد چند ارگان بدن
تومورهای نورواندوکرین(مثل سرطان مدولای تیروئید)
سوختگی های شدید
ترومای شدید
درمان با آنتی بادی های (که برای جلوگیری از حمله سلول های T به بافت پیوندی استفاده می شود) و دیگر داروهای تنظیم کننده ترشح سایتوکاین ها
تهیه شده توسط:
واحد تحقیق و توسعه (R & D) آزمایشگاه پاتوبیولوژی وحید
سید محمد حسین حسینی، دکتر محمد وحید دستجردی
تهیه شده توسط واحد تحقیق و توسعه (R & D) آزمایشگاه پاتوبیولوژی وحید: سید محمد حسین حسینی، دکتر محمد وحید دستجردی
:References
1. A Manual of Laboratory and Diagnostic Tests
2. Principles of Biochemistry- Lehninger
Laboratory test handbook,3rd edition ,David S.Jacobs
World Health Organization (WHO). Coronavirus disease 2019 (COVID-19) Situation report – 124. [accessed 24 May 2020].
Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. 2020;323:1061–1069. doi: 10.1001/jama.2020.1585.
Zhang JJ, Dong X, Cao YY, Yuan YD, Yang YB, Yan YQ. Clinical characteristics of 140 patients infected with SARS-CoV-2 in Wuhan, China. 2020 Feb 19 doi: 10.1111/all.14238. [Epub ahead of print].
Lu R, Zhao X, Li J, Niu P, Yang B, Wu H. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. 2020;395:565–574. doi: 10.1016/S0140-6736(20)30251-8.
Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. 2020;395:497–506. doi: 10.1016/S0140-6736(20)30183-5.
Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, He JX. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020;382:1708–1720. doi: 10.1056/NEJMoa2002032.
Lippi G, Plebani M. Procalcitonin in patients with severe coronavirus disease 2019 (COVID-19): a meta-analysis. Clin Chim Acta. 2020;505:190–191. doi: 10.1016/j.cca.2020.03.004.
State Council of The People’s Republic of China . 2020. The notice of launching guideline on diagnosis and treatment of the novel coronavirus pneumonia (6th edition)[in Chinese] [accessed 2 April 2020].
Lippi G, Cervellin G. Procalcitonin for diagnosing and monitoring bacterial infections: for or against? Clin Chem Lab Med. 2018;56:1193–1195. doi: 10.1515/cclm-2018-0312.
Lippi G, Plebani M. Laboratory abnormalities in patients with COVID-2019 infection. Clin Chem Lab Med. 2020 Mar 3 doi: 10.1515/cclm-2020-0198.