ANA Patterns
آنتی بادی های ضد هسته، عوامل مهمی در تشخیص طیف گسترده ای از بیماری های اتوایمیون هستند. روش های مختلفی برای شناسایی این آنتی بادی ها وجود دارد از جمله الایزا، ایمنوفلوئورسانس (IF) ، مالتیپلکس ایمونواسی (multiplex immunoassay)، فلوسایتومتری، line/dot blot، میکرواری و غیره. معرفی رده سلولی اپیتلیال انسانی نوع 2 (cells HEP-2) بعنوان یک سوبسترا برای آزمایش ANA به روش ایمنوفلوئورسانس (IF)، این دیدگاه را ایجاد کرد که علاوه بر الگوهای هسته ای، الگوهای سیتوپلاسمی و الگوهای سلول میتوزی نیز قابل شناسایی هستند. اتوآنتیبادی هایی که در برابر اجزای سلولی ایجاد می شوند، مارکرهای مهمی برای تشخیص و افتراق بیماریهای اتوایمیون سیستمیک هستند. استاندارد طلایی (gold standard) برای تشخیص آنتی بادی های ضد هستهای و اتوآنتی بادیهای ضد سیتوپلاسمی، ایمنوفلوئورسانس غیرمستقیم روی سلولهای HEP-2 است. بیش از 100 اتوآنتیژن بر روی سلول های Hep-2 وجود دارد که مهمترین آنها عبارتند از:
پلی نوکلئوتیدها | Double-stranded DNA, single-stranded DNA, RNA |
هیستون ها | H1, H2A, H2B, H3, H4, H2A-H2B complex |
ریبونوکلئوپروتئین ها | U1-(n)RNP, Sm, SS-A (Ro), SS-B (La) |
آنتی ژن های هستک | U3-(n)RNP/fibrillarin, RNA polymerase I, PM-Scl (PM-1),7-2-RNP (To), 4-6-S-RNA, NOR-90 (nucleolar organiser) |
سانترومرها | Kinetochore proteins |
سایر پروتئین ها | Topoisomerase I (Scl-70), PCNA (cyclin I), nuclear granules, Ku, Mi-2, lamins, lamin receptors |
وجود آنتی بادی های ضد هسته ای (ANA) در خون بیمار، یک یافته ارزشمند در بسیاری از بیماری ها، به ویژه بیماری های روماتیسمی (اما نه منحصرا) است. در ادامه به میزان شیوع ANA در بیماری های مختلف اشاره می گردد:
بیماری اتوایمیون | شیوع ANA (درصد) |
لوپوس اریتماتوز سیستمیک (SLE) | 95 – 100 |
لوپوس اریتماتوز ناشی از دارو | 100 |
بیماری بافت همبند مختلط یا سندروم Sharp | 100 |
آرتریت روماتوئید | 20 – 40 |
سایر بیماری های روماتیسمی | 20 – 50 |
اسکلروز سیستمیک پیشرونده | 85 – 95 |
پلی میوزیت/درماتومیوزیت | 30 – 50 |
سندروم شوگرن | 70 – 80 |
هپاتیت اتوایمیون | 30 – 40 |
کولیت اولسراتیو | 26 |
آنتی بادی های مختلف بسته به موقعیت سلولی و خصوصیات آنتی ژنیک هدف آنها، الگوهای رنگ آمیزی مشخصی روی سلول ها ایجاد می کنند. توافق بینالمللی الگوهای آنتی بادی ضد هسته ای، آنتی بادی های شناسایی شده بر روی سلولهای HEp-2 را به سه دسته اصلی تقسیم میکند: الگوهای فلوئورسانس هسته ای، سیتوپلاسمی و میتوزی. هر کدام از این دسته ها به گروه ها و زیر گروه های مختلف تقسیم می شوند. به هر الگو یک کد الگوی ضد سلولی یا Anti-cell (AC) از AC-1 تا AC-29 اختصاص داده شده است. طبقه بندی این الگوها، اطلاعات مفیدی در خصوص آنتی ژن های ایجاد شده و در نتیجه شناسایی بیماری احتمالی فراهم می کند. شکل زیر این کدگذاری را بصورت طبق بندی شده نشان می دهد:
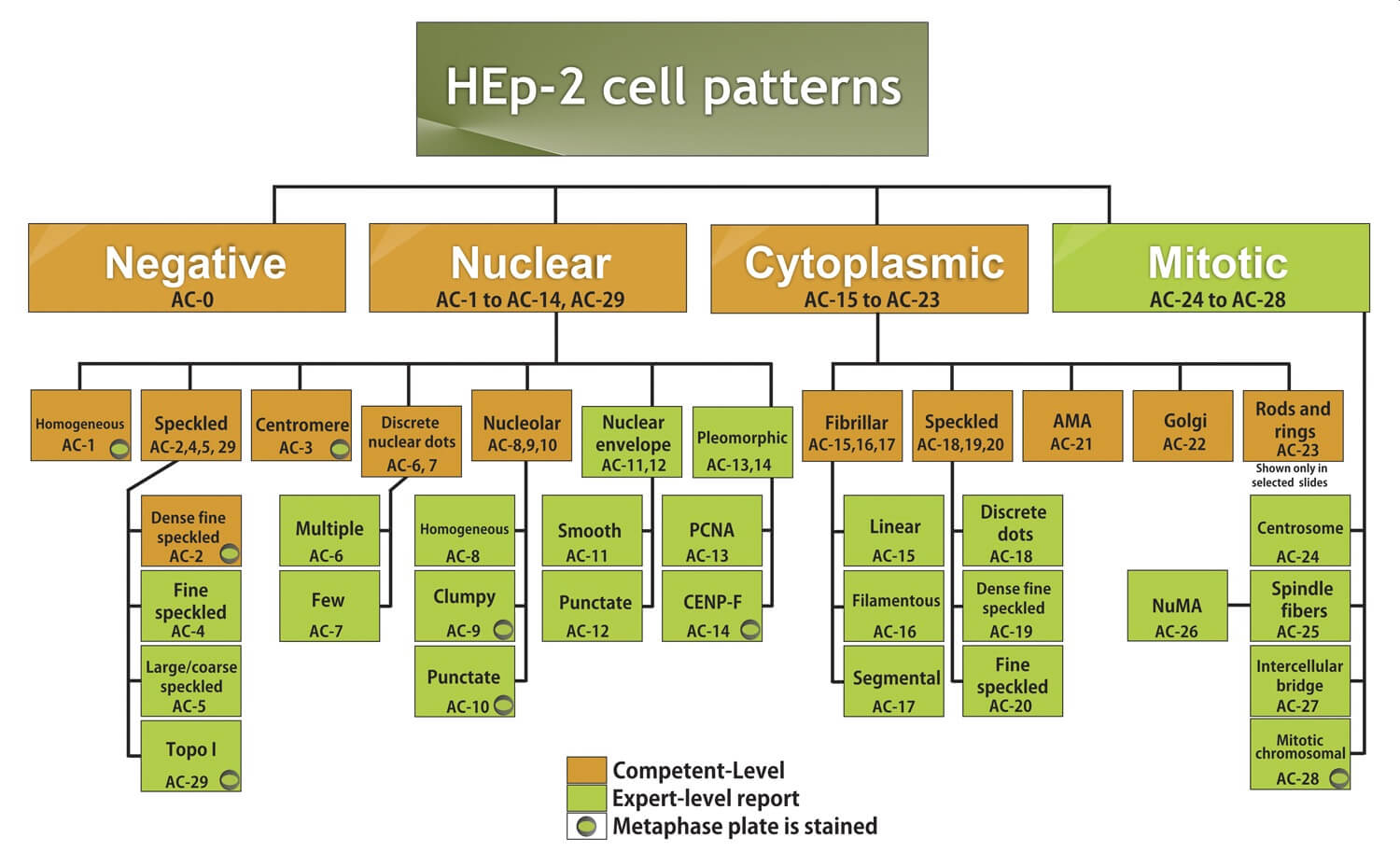
الگوهای هسته ای
الگوهای هسته ای شامل کدهای AC-1 تا AC-14 و همچنین AC-29 (اخیرا شناسایی شده) هستند که در گروه های اصلی هوموژنوس (Homogeneous)، لکه دار (Speckled)، سانترومر (Centromere)، هستکی (nucleolar) ، پاکت هسته ای (Nuclear envelope) و پلئومورفیک (Pleomorphic) طبقه بندی می شوند. آنتی بادی های این گروه به ویژه در بیماری های روماتیسمی اتوایمیون سیستمیک (systemic autoimmune rheumatic diseases) ، لوپوس اریتماتوز سیستمیک (SLE) ، بیماری های بافت همبند، سندروم شوگرن، اسکلروزیس سیستمیک، پلی میوزیت و درماتومیوزیت دیده می شوند.
الگوهای سیتوپلاسمی
الگوهای سیتوپلاسمی از AC-15 تا AC-23 کدگذاری شده اند که در گروه های اصلی فیبریلی (fibrillar) ، لکه دار (speckled) ، مشبک/شبه میتوکندری (reticular/mitochondria-like) ، قطبی/شبه گلژی (Polar/Golgi-like)، میله ای و حلقه ای (Rods and rings) طبقه بندی می شوند. آنتی بادی های سیتوپلاسمی با بیماری های لوپوس اریتماتوز سیستمیک، پلی میوزیت/درماتومیوزیت ، کلانژیت صفراوی اولیه و … مرتبط هستند.
الگوهای میتوزی
الگوهای میتوزی از AC-24 تا AC-28 کدگذاری شده اند. آنتی بادی های میتوزی ندرتا در بیماری هایی مانند اسکلروزیس سیستمیک، لوپوس اریتماتوز سیستمیک، سندروم شوگرن و پدیده رینود دیده می شوند.
ردیابی آنتی بادی اختصاصی
اتوآنتی بادی ها با استفاده از تست های اختصاصی مختلفی از جمله ایمنوفلوئورسانس غیرمستقیم با آنتی ژن خالص شده یا روش های ایمونواسی مانند الیزا و ایمونوبلات قابل تشخیص و افتراق هستند. در روش ایمنوفلوئورسانس غیرمستقیم، سوبسترا های اختصاصی از جمله SS-A, SS-B, Scl-70, Jo-1, ribosomal P-proteins, RNP/Sm, Sm بر روی سلول های Hep-2 بعنوان صفحات Biochip قابل آنالیز هستند. پروفایل های الایزا و ایمونوبلات، ترکیبی از آنتی ژن های مختلف را برای شناسایی اختصاصی تعداد زیادی از آنتی بادی ها فراهم کرده اند.
تائید ANA
برای تائید تست ANA باید از آزمایش های ANA confirmatory استفاده شود. در این روش ها اتوآنتی بادی های اختصاصی قابل آنالیز هستند. در این خصوص می توان به آزمایش ANA Profile یا ANA Panel با استفاده از روش های الایزا، Multiplex flow immunoassay ، immunoblotting و … اشاره نمود. در ادامه به الگوهای هسته ای، سیتوپلاسمی و میتوزی اتوآنتی بادی ضد هسته ای با روش فلوئورسنت غیر مستقیم بر اساس کدگذاری بین المللی و همچنین ارتباط بالینی هر کدام از آنها با بیماری های اتوایمیون مختلف پرداخته خواهد شد:
الگوهای هستهای
کد AC-1 : الگوی هوموژنوس هسته ای (Nuclear homogeneous)
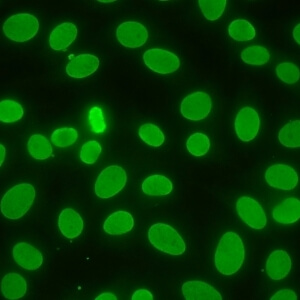
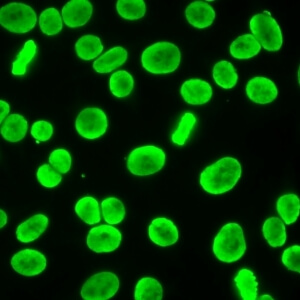
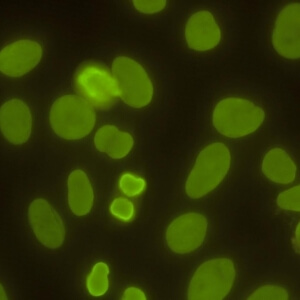
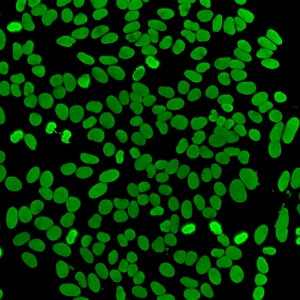
- نام قبلی: الگوی منتشر
- توضیحات: فلوئورسانس هوموژنوس و منظم در همه نوکلئوپلاسم. هستک ممکن است بسته به سوبسترای سلولی رنگ آمیزی شود یا رنگ آمیزی نشود. توده کروماتین سلول هایی که در مرحله میتوز قرار دارند (متافاز، آنافاز و تلوفاز)، بصورت هوموژنوس شفاف بشدت رنگ می گیرد.
- ارتباط آنتی ژنی: DNA دو رشته ای، نوکلئوزوم ها، هیستون ها
- ارتباط بالینی: در بیماران مبتلا به لوپوس اریتماتوز سیستمیک (SLE)، هپاتیت مزمن اتوایمیون یا آرتریت ایدیوپاتیک جوانان
کد AC-2 : الگوی متراکم ظریف لکه دار هسته ای (Nuclear dense fine speckled)
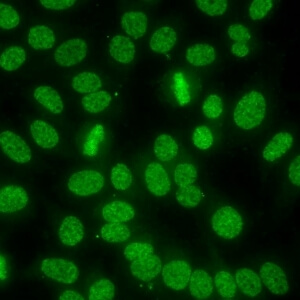
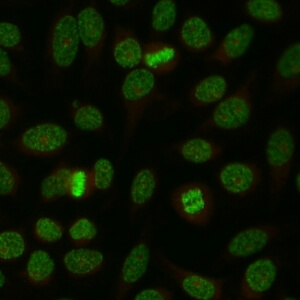
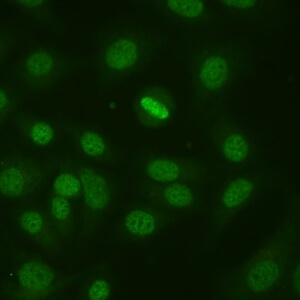
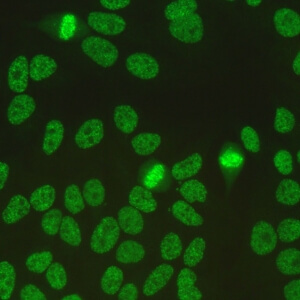
- نام قبلی: –
- توضیحات: الگوی لکه دار با هتروژنیسیته مشخص در سایز، درخشندگی و پراکندگی لکه ها که در سرتاسر هسته اینترفازی توزیع شده است.
- ارتباط آنتی ژنی: DFS70/LEDGF
- ارتباط بالینی: معمولاً به عنوان HEP-2 IIFA مثبت با تیتر بالا، در افراد به ظاهر سالم یا در بیمارانی که به بیماری روماتیسمی اتوایمیون سیستمیک مبتلا نیستند، مشاهده می شود.
کد AC-3 : الگوی سانترومر (Centromere)
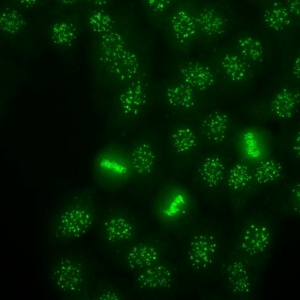
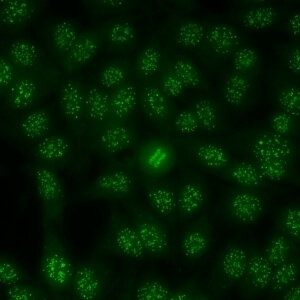
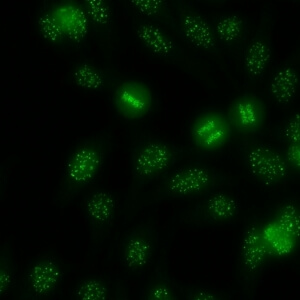
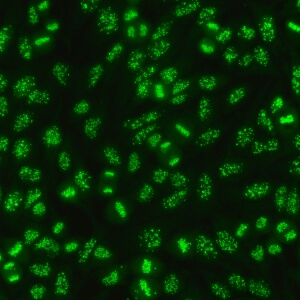
- نام قبلی: Kinetochore
- توضیحات: لکه های خشن (coarse) مجزا (40 تا 80 عدد در هر سلول) که در سلولهای اینترفاز پراکنده شده و در توده کروماتین درون سلولهای میتوزی قرار گرفته اند. مثال: anti-CENP-B
- ارتباط آنتی ژنی: CENP-A/B (C)
- ارتباط بالینی: معمولاً در بیماران با اسکلروزیس سیستمیک محدود پوستی مشاهده می شود.
کد AC-4 : الگوی لکه دار ظریف هسته ای (Nuclear fine speckled)
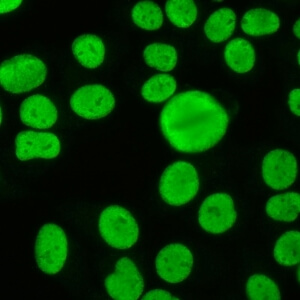
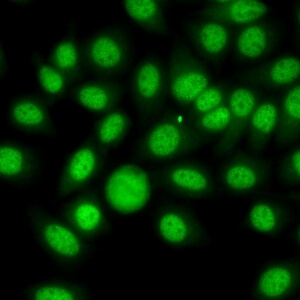
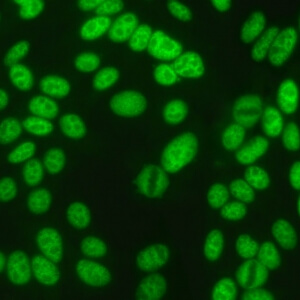

- نام قبلی: الگوی گرانولار ظریف
- توضیحات: لکههای ظریف و کوچک در سرتاسر نوکلئوپلاسم. هستکها ممکن است رنگآمیزی شود یا رنگآمیزی نشود. سلولهای میتوزی (متافاز، آنافاز و تلوفاز)، تودههای کروماتینی دارد که رنگآمیزی نمی شود. مثال: Anti-SS-A/Ro, Anti-SS-B/La
- ارتباط آنتی ژنی: SS-A/Ro, SS-B/La, Mi-2, TIF1γ, TIF1β, Ku
- ارتباط بالینی: با درجات مختلفی در بیماری روماتیسمی اتوایمیون سیستمیک، به ویژه سندروم شوگرن، لوپوس اریتماتوز سیستمیک، لوپوس اریتماتوز جلدی تحت حاد، لوپوس اریتماتوز نوزادان، انسداد مادرزادی قلب، درماتومیوزیت، اسکلروزیس سیستمیک و سندروم اورلپ میوپاتی اتوایمیون – اسکلروزیس سیستمیک وجود دارد.
کد AC-5 : الگوی بزرگ/خشن لکه دار هسته ای (Nuclear large/coarse speckled)
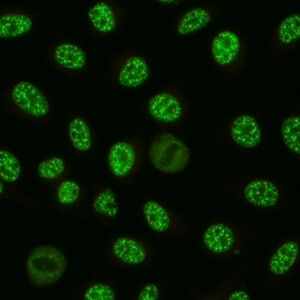
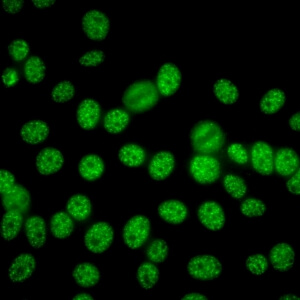
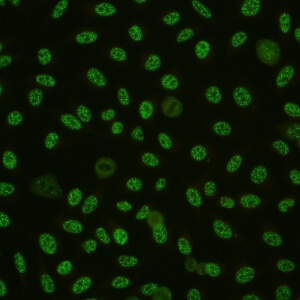
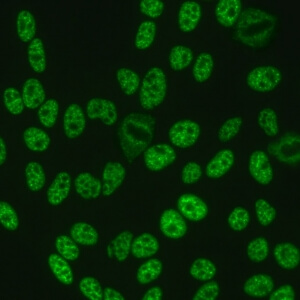
- نام قبلی: الگوی اسپلایسوزوم/ماتریکس هسته ای
- توضیحات: لکه های خشن در سرتاسر نوکلئوپلاسم. هستکها ممکن است رنگآمیزی شود یا رنگآمیزی نشود. سلولهای میتوزی (متافاز، آنافاز و تلوفاز)، تودههای کروماتینی دارد که رنگآمیزی نمی شود. مثال: anti-Sm, anti-U1 RNP
- ارتباط آنتی ژنی: hnRNP, U1RNP, Sm, RNA polymerase III
- ارتباط بالینی: با درجات مختلفی در بیماری روماتیسمی اتوایمیون سیستمیک، به ویژه لوپوس اریتماتوز سیستمیک، بیماری بافت همبند مختلط، اسکلروزیس سیستمیک، سندروم اورلپ میوپاتی اتوایمیون – اسکلروزیس سیستمیک و بیماری تمایز نیافته بافت همبند (بیماران دارای علایم روماتیسمی ولی بدون معیارهای تشخیصی یکی از بیماری های روماتیسمی اتوایمیون سیستمیک) وجود دارد.
کد AC-6 : الگوی نقاط هسته ای پرتعداد (Multiple nuclear dots)
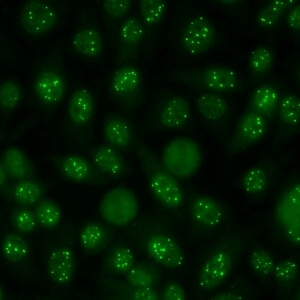
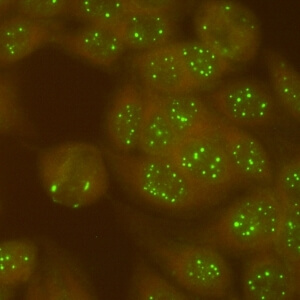
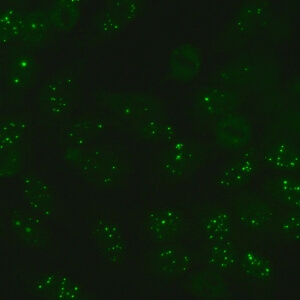
- نام قبلی: 6 – 20 nuclear dots, NSpI, PML bodies
- توضیحات: لکه های قابل شمارش هسته ای مجزا (6 تا 20 نقطه هسته ای در هر سلول). مثال: SP-100
- ارتباط آنتی ژنی: Sp-100, PML proteins, MJ/NXP-2
- ارتباط بالینی: در طیف گسترده ای از بیماری های اتوایمیون شامل کلانژیت صفراوی اولیه، میوپاتی اتوایمیون، درماتومیوزیت و همچنین سایر شرایط التهابی
کد AC-7 : الگوی نقاط هسته ای کم تعداد (Few nuclear dots)
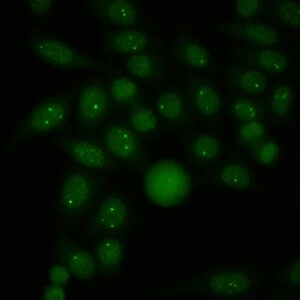
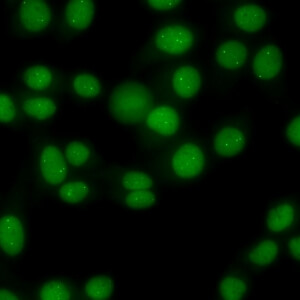
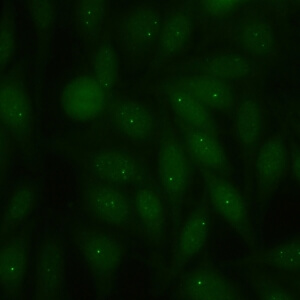
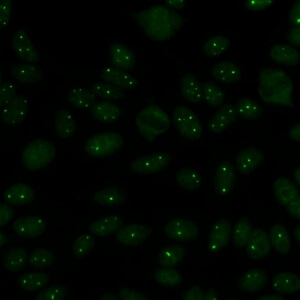
- نام قبلی: الگوی 1 تا 6 نقطه هسته ای، جسم پیچ خورده، اجسام Cajal
- توضیحات: لکه های قابل شمارش هسته ای مجزا (در اکثر سلول ها 1 تا 6 نقطه هسته ای در هر سلول وجود دارد). این لکه ها به عنوان جسم پیچ خورده یا اجسام Cajal شناخته می شوند. مثال: ضد p80-Coilin
- ارتباط آنتی ژنی: p80-coilin, SMN
- ارتباط بالینی: الگوی AC-7 ارزش اخباری مثبت پائینی برای هر بیماری ای دارد.
کد AC-8 : الگوی هستکی هوموژنوس (Homogeneous nucleolar)
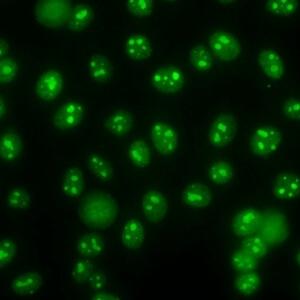
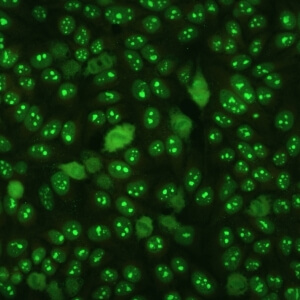
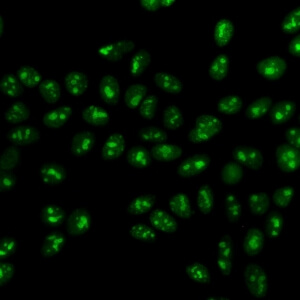
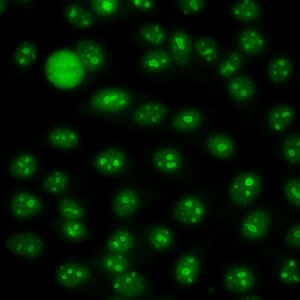
- نام قبلی: –
- توضیحات: فلوئورسانس منتشر در کل هستک، در حالی که صفحه متافازی رنگ نمی گیرد. مثال: anti-PM-Scl, anti-Th/To.
- ارتباط آنتی ژنی: PM/Scl-75, PM/Scl-100, Th/To, B23/nucleophosmin, nucleolin, No55/SC65
- ارتباط بالینی: در بیماران مبتلا به اسکلروزیس سیستمیک، سندروم اورلپ میوپاتی اتوایمیون – اسکلروزیس سیستمیک و در بیمارانی با تظاهرات بالینی سایر بیماری های روماتیسمی اتوایمیون سیستمیک
کد AC-9 : الگوی هستکی توده ای (Clumpy nucleolar)
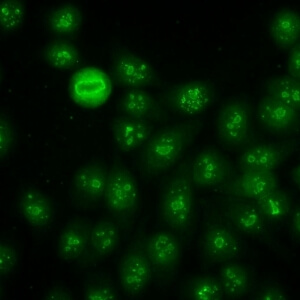
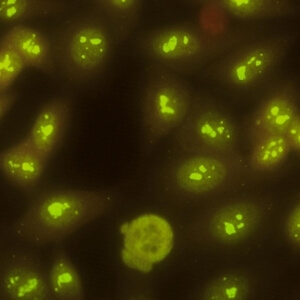
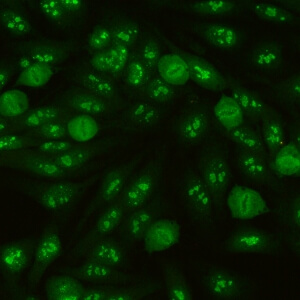
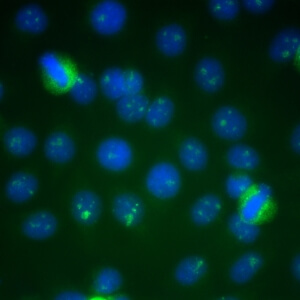
- نام قبلی: هستکی لکه دار
- توضیحات: به صورت متراکم توزیع شده اما دانه های متمایزی در هستک های سلول اینترفازی مشاهده می شود. در سلولهای متافازی، حداکثر 5 جفت ناحیه سازمان دهنده هستکی در جسم کروماتینی دیده می شود. سیتوپلاسم سلولهای میتوزی ممکن است به مقدار جزئی مثبت باشد. مثال: anti-NOR-90 ، anti-RNA polymerase I
- ارتباط آنتی ژنی: RNA polymerase I, hUBF/NOR-90
- ارتباط بالینی: الگوی AC-10 در شرایط مختلفی دیده می شود از جمله اسکلروزیس سیستمیک، پدیده رینود، سندروم شوگرن و سرطان.
کد AC-10 : الگوی هستکی سوراخ سوراخ (Punctate nucleolar)
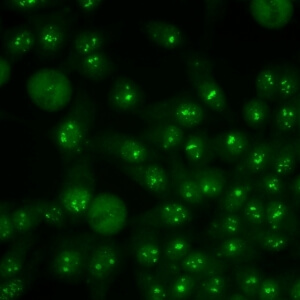
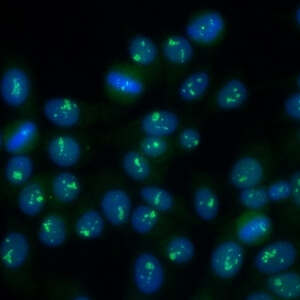
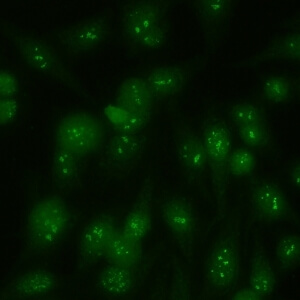
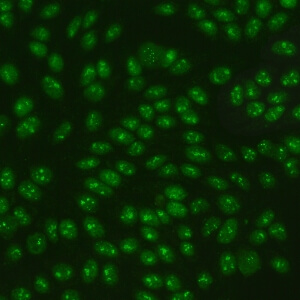
- نام قبلی: هستکی لکه دار
- توضیحات: به صورت متراکم توزیع شده اما دانه های متمایزی در هستک های سلول اینترفازی مشاهده می شود. در سلولهای متافازی، حداکثر 5 جفت ناحیه سازمان دهنده هستکی در جسم کروماتینی دیده می شود. سیتوپلاسم سلولهای میتوزی ممکن است به مقدار جزئی مثبت باشد. مثال: anti-NOR-90 ، anti-RNA polymerase I
- ارتباط آنتی ژنی: RNA polymerase I, hUBF/NOR-90
- ارتباط بالینی: الگوی AC-10 در شرایط مختلفی دیده می شود از جمله اسکلروزیس سیستمیک، پدیده رینود، سندروم شوگرن و سرطان.
کد AC-11 : الگوی پاکت هسته ای صاف (Smooth nuclear envelope)
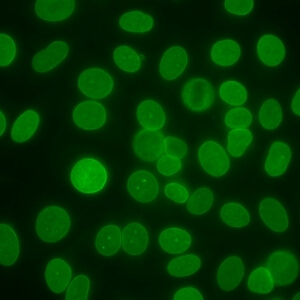
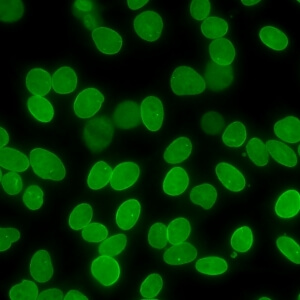
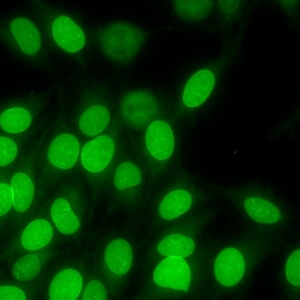
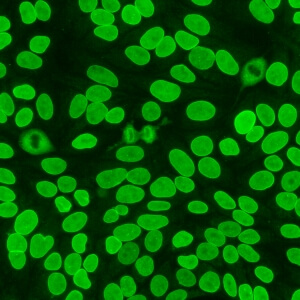
- نام قبلی: لبه هسته ای، غشای هسته ای، غشایی
- توضیحات:
- هسته بصورت هوموژنوس رنگ می گیرد و شدت رنگ در لبه بیرونی هسته بیشتر است در صورتی که صفحات کروماتینی متافاز و آنافاز رنگ نمی گیرند. در نقاطی که سلولهای مجاور در تماس با یکدیگر قرار می گیرند، فلورسانس با شدت ویژه ای دیده می شود. مثال: anti-lamin B
- ارتباط آنتی ژنی: lamins A,B,C, or lamin-associated proteins
- ارتباط بالینی: الگوی AC-11 به ندرت در آنالیز معمول اتوآنتی بادی یافت می شود و در سایتوپنی اتوایمیون، بیماریهای کبدی اتوایمیون، اسکلرودرمی خطی، سندروم آنتی فسفولیپید و بیماری های روماتیسمی اتوایمیون سیستمیک دیده می شود.
کد AC-12 : الگوی پاکت هسته ای سوراخ سوراخ (Punctate nuclear envelope)
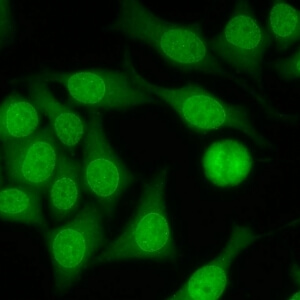
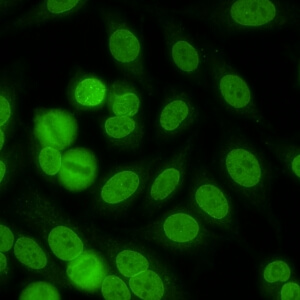
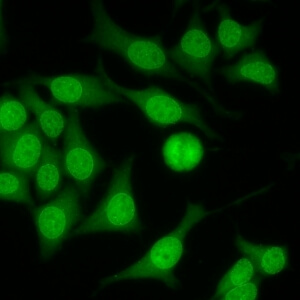
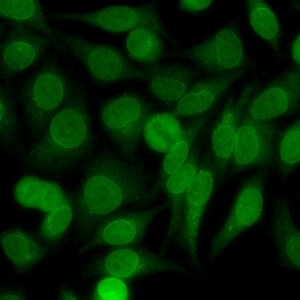
- نام قبلی: منافذ غشای هسته
- توضیحات: پاکت هسته ای با نمای رنگ آمیزی سوراخ سوراخ در سلول های اینترفاز و در نقاطی که سلولهای مجاور در تماس با یکدیگر قرار می گیرند، فلورسانس با شدت ویژه ای دیده می شود. صفحات کروماتینی آنافاز و متافاز رنگ نمی گیرند. مثال: anti-gp210
- ارتباط آنتی ژنی: پروتئین های کمپلکس منافذ هسته ای یعنی gp210
- ارتباط بالینی: در بیماران مبتلا به کلانژیت صفراوی اولیه و همچنین بیماران مبتلابه سایر بیماریهای اتوایمیون کبد و بیماری های روماتیسمی اتوایمیون سیستمیک
کد AC-13 : الگوی شبه آنتی ژن هسته ای سلول در حال تکثیر (proliferating cell nuclear antigen-like)
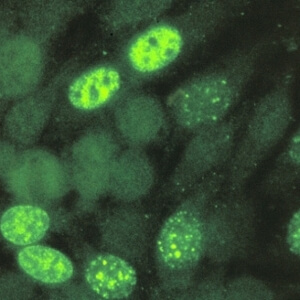
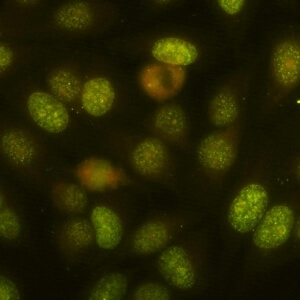
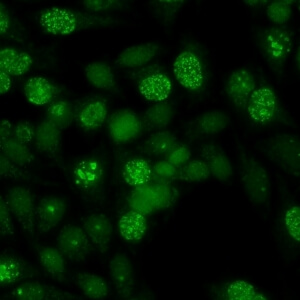
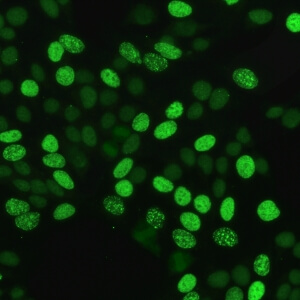
- نام قبلی: –
- توضیحات: رنگ آمیزی نوکلئوپلاسمی لکه های چند شکلی با تفاوت در اندازه و درخشندگی لکه ها. در اینترفاز، برخی سلولها منفی هستند (فاز G1)، برخی از آنها به شدت رنگ می گیرند (فاز S) و برخی دیگر از سلولها، لکه های پراکنده و بسیار کم تعداد که در آنها هستک ها گاها رنگ می گیرند (اواخر فاز S و اوایل فاز G2). سلول های میتوزی رنگ نمی گیرند.
- ارتباط آنتی ژنی: PCNA
- ارتباط بالینی: الگوی AC-13 قبلا برای لوپوس اریتماتوز سیستمیک بسیار اختصاصی در نظر گرفته می شد، اما این اختصاصیت مورد بحث است.
کد AC-14 : الگوی پروتئین f مرتبط با سانترومر (centromere-associated protein F-like)
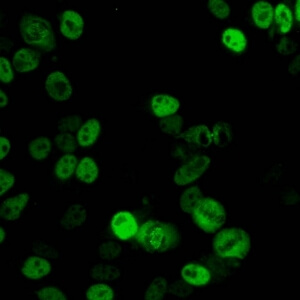
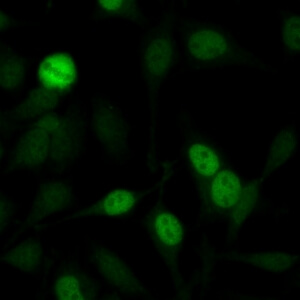
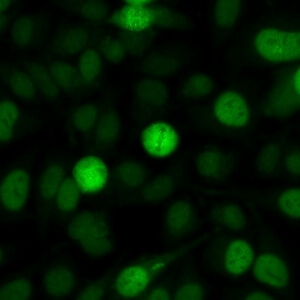
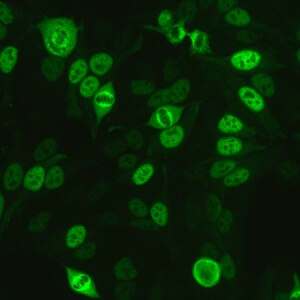
- نام قبلی: MSA-3, NSp-II
- توضیحات: الگوی لکه دار هسته ای با تنوع قابل توجه در شدت رنگ پذیری (شدیدترین رنگ پذیری در فاز G2 و ضعیف ترین رنگ پذیری یا عدم رنگ پذیری در فاز (G1. سانترومرها فقط در پرومتافاز و متافاز مثبت هستند که در آنها نقاط كوچك همردیف و ضعیف دیده می شود. در سلول های پرومتافاز، پاکت هسته ای غالباً بصورت ضعیف رنگ می گیرد. طی آنافاز و تلوفاز، بعضی از سرم ها در حلقه واقع در قسمت میانی سلول یعنی جایی که سلول های دختری جدا می شوند، شدیدا رنگ می گیرند. سیتوپلاسم اطراف سلولهای میتوزی بصورت منتشر رنگ می گیرند.
- ارتباط آنتی ژنی: CENP-F
- ارتباط بالینی: اکثر سرمهایی که الگوی AC-14 را نشان می دهند، مربوط به بیماران مبتلا به انواع شرایط نئوپلاستیک (سینه، ریه، کولون، لنفوم، تخمدان مغز) است.
کد AC-29 : الگوی شبه DNA توپوایزومراز I (DNA topoisomerase I-like)
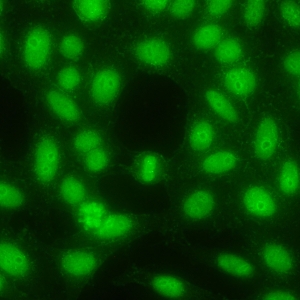
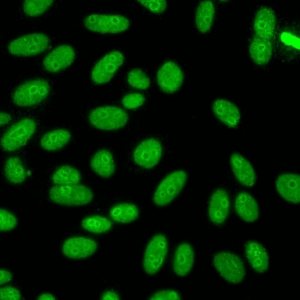
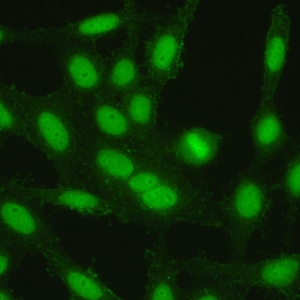
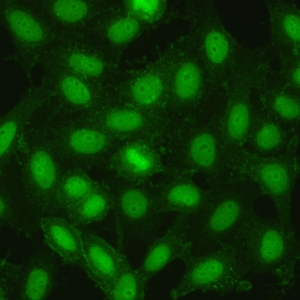
- نام قبلی: Scl-70-like, Scl-86, DNA Topo I
- توضیحات: الگوی الگوی شبه DNA توپوایزومراز I می تواند شامل رنگ آمیزی پنج ناحیه درون سلولی باشد:
1) رنگ آمیزی هسته ای الگوی AC-4 با لکه های ظریف برجسته در سلول های اینترفازی.
2) رنگ آمیزی لکه دار یکنواخت ظریف پررنگ کروماتین متراکم شده در سلول های میتوزی. بسته به رقت سرم مورد استفاده، رنگ پذیری کروماتین میتوزی ممکن است هوموژنوس دیده شود.
3) رنگ آميزی ناحيه سازماندهنده هستکی مرتبط با کروموزوم های متراکم شده در سلول ها ميتوزی. این رنگ آميزی ناحيه سازماندهنده هستکی ممکن است توسط رنگ آمیزی روشن کروموزومی پنهان شود زیرا نواحی سازماندهنده هستکی همیشه در یک صفحه کانونی قرار ندارند.
4) رنگ آمیزی سیتوپلاسمی ضعیف در سلول های اینترفاز (و میتوزی) یک شبکه ظریف را نشان می دهد که از ناحیه اطراف هسته ای به سمت غشای پلاسما امتداد می یابد. به طور کلی در تیتراسیون سرم، هر چه رقت بالاتر می رود، رنگ آمیزی سیتوپلاسمی نسبتا برجسته تر دیده می شود.
5) رنگ آمیزی هستکی متغیر که بصورت یک هستک سوراخ سوراخ یا رنگ پذیری اطراف هسته در سلول های اینترفاز دیده می شود. رنگ آمیزی هستکی یک ویژگی ثابت و همیشگی این الگو نیست.
- ارتباط آنتی ژنی: DNA topoisomerase I
- ارتباط بالینی: الگوی AC-29 برای اسکلروزیس سیستمیک بسیار اختصاصی است، بخصوص در مورد اسکلروزیس سیستمیک پوستی منتشره و فرم های مهاجم تر اسکلروزیس سیستمیک.
الگوهای سیتوپلاسمی
کد AC-15 : الگوی فیبریلی خطی سیتوپلاسمی (Cytoplasmic fibrillar linear)
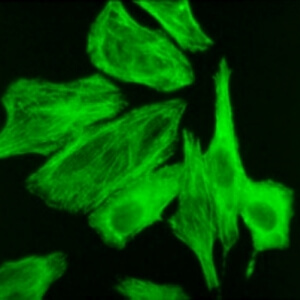
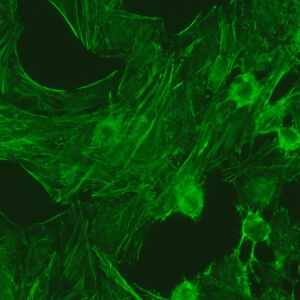
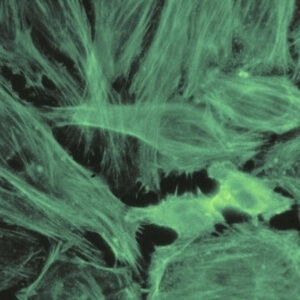
- نام قبلی: شبه اکتین
- توضیحات: این الگو با فیبرهای سایتواسکلتی، گاهی اوقات با رسوبات گرانولار کوچک و ناپیوسته مشخص می شود. رنگ آمیزی معمولی، رشته های مخطط اکتین که در محور طولانی سلول امتداد می یابد را نشان می دهد.
مثال: anti-actin, anti-non-muscle myosin
- ارتباط آنتی ژنی: actin, non-muscle myosin
- ارتباط بالینی: در بیماران مبتلا به هپاتیت اتوایمیون نوع1 ، عفونت مزمن هپاتیت C و بیماری سلیاک (ایزوتایپ IgA) مشاهده می شود. به ندرت در بیماری های روماتیسمی اتوایمیون سیستمیک دیده می شود.
کد AC-16 : الگوی فیبریلی فیلامنتی سیتوپلاسمی (Cytoplasmic fibrillar filamentous)
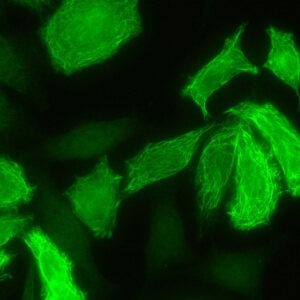
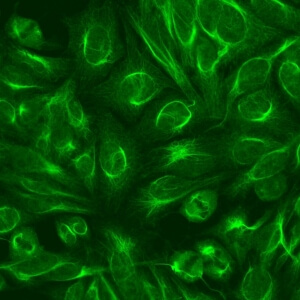
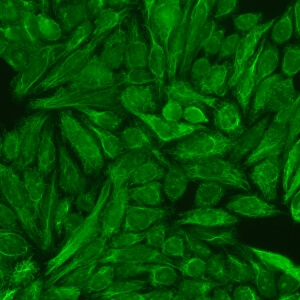
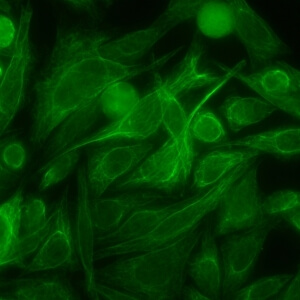
- نام قبلی: –
- توضیحات: رنگ آمیزی میکروتوبول ها و فیلامنت های حدواسط که از لبه هسته بیرون می آیند. مثال: anti-cytokeratin, anti-vimentin, anti-tropomyosin
- ارتباط آنتی ژنی: vimentin, cytokeratins, tropomyosin
- ارتباط بالینی: در بیماری های مختلف یافت می شود، اما معمولا در بیماری های روماتیسمی اتوایمیون سیستمیک دیده نمی شود.
کد AC-17 : الگوی فیبریلی قطعه قطعه سیتوپلاسمی (Cytoplasmic fibrillar segmental)
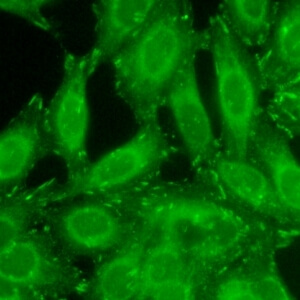
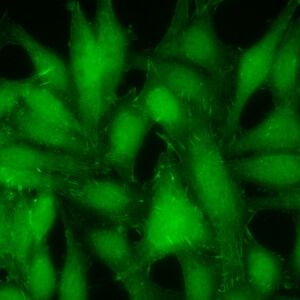
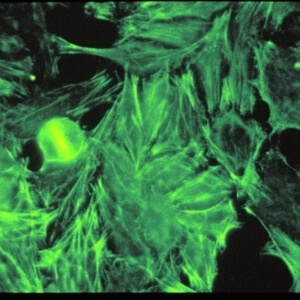
- نام قبلی: –
- توضیحات: تعداد زیادی قطعات کوتاه، اجسام متراکم متناوب، در امتداد فیبرهای استرس. مثال: anti-alpha-actinin, anti-vinculin
- ارتباط آنتی ژنی: alpha-actinin, vinculin
- ارتباط بالینی: به ندرت یافت می شود
کد AC-18 : الگوی نقاط مجزای سیتوپلاسمی/اجسام شبه GW (Cytoplasmic discrete dots/GW body-like)
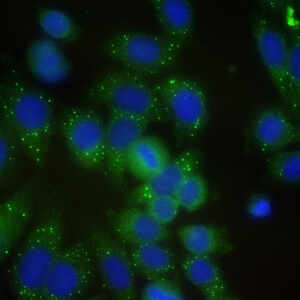
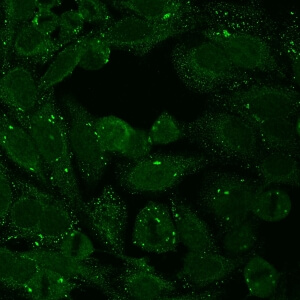
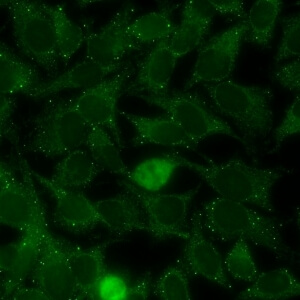
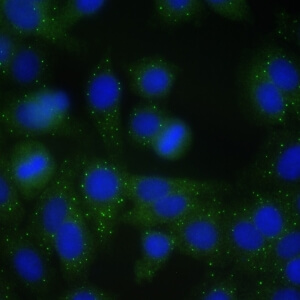
- نام قبلی: GW body, processing body, lysosome
- توضیحات: رنگ آمیزی اجسام GW در سیتوپلاسم سلولهای اینترفاز با تعداد زیاد در سلولهایی که در اواخر فاز S و فاز G2 قرار دارند. مثال: anti-GW182, anti-Su/Ago2
- ارتباط آنتی ژنی: GW182, Su/Ago2
- ارتباط بالینی: اتوآنتی بادی هایی که الگوی AC-18 را نشان می دهند، در بیماری های روماتیسمی اتوایمیون سیستمیک و در انواعی از سایر بیماری ها گزارش شده اند.
کد AC-19 : الگوی لکه دار ظریف متراکم سیتوپلاسمی (Cytoplasmic dense fine speckled)
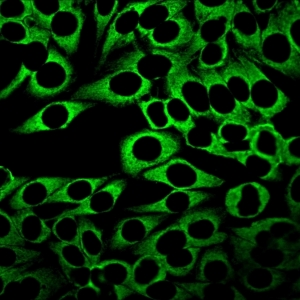
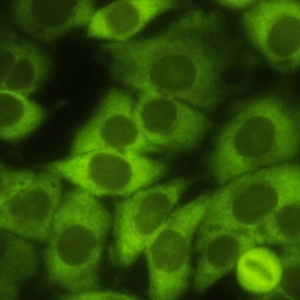
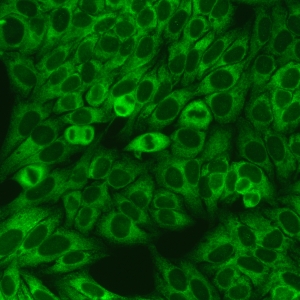
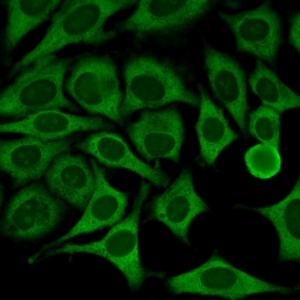
- نام قبلی: هوموژنوس سیتوپلاسمی
- توضیحات: این الگو بصورت تیره (شبیه ابر) و تقریبا هوموژنوس در سرتاسر سیتوپلاسم دیده می شود. مثال: anti-PL-7
- ارتباط آنتی ژنی: PL-7, PL-12, ribosomal P proteins
- ارتباط بالینی: در بیماران مبتلا به لوپوس اریتماتوز سیستمیک و سندرم آنتی سنتتاز (یکی از زیر مجموعه های میوپاتی اتوایمیون)، بیماری بینابینی ریه، پلی آرتریت، پدیده رینود و بیماری دست مکانیک یافت می شود.
کد AC-20 : الگوی لکه دار ظریف سیتوپلاسمی (Cytoplasmic fine speckled)
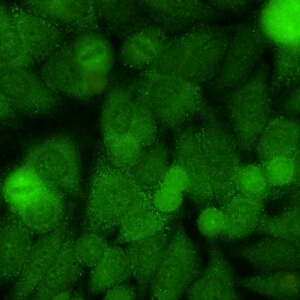
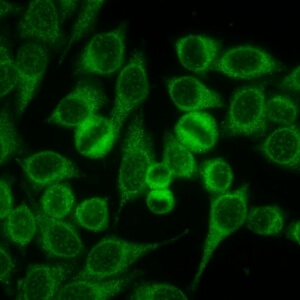
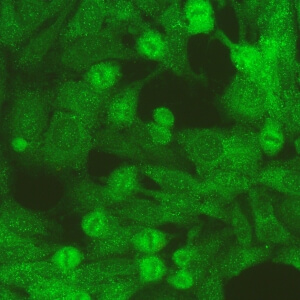
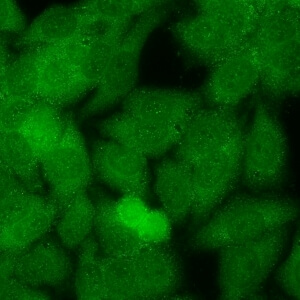
- نام قبلی: لکه دار سیتوپلاسمی
- توضیحات: لکه های کوچک پراکنده در سیتوپلاسم اکثرا با بکگراند هوموژنوس یا لکه دار ظریف متراکم. مثال: anti-Jo-1
- ارتباط آنتی ژنی: Jo-1/histidyl-tRNA synthetase
- ارتباط بالینی: در بیماران مبتلا به سندرم آنتی سنتتاز (یکی از زیر مجموعه های میوپاتی اتوایمیون)، بیماری بینابینی ریه، پلی آرتریت، پدیده رینود و بیماری دست مکانیک یافت می شود.
کد AC-21 : الگوی مشبک سیتوپلاسمی/آنتی بادی های ضد میتوکندری (Cytoplasmic reticular/antimitochondrial antibodies)
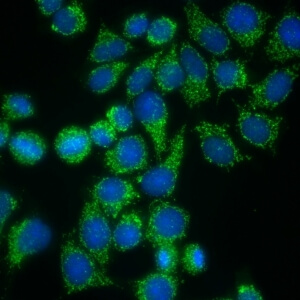
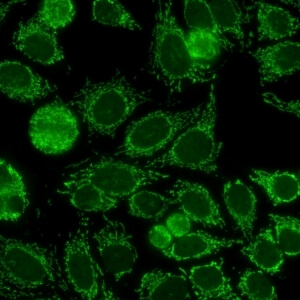
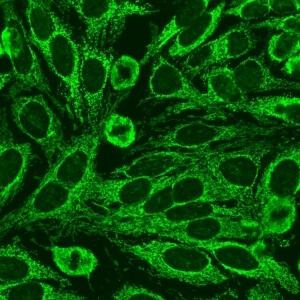
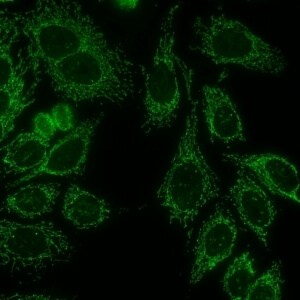
- نام قبلی: شبه میتوکندری
- توضیحات: رنگ آمیزی فیلامنتی گرانولار خشن در سرتاسر سیتوپلاسم. مثال: آنتی بادی های ضد میتوکندری
- ارتباط آنتی ژنی: PDC-E2/M2, BCOADC-E2, OGDC-E2, E1α subunit of PDC, E3BP/protein X
ارتباط بالینی: معمولا در کلانژیت صفراوی اولیه یافت می شود ولی در اسکلروزیس سیستمیک شامل سندروم اورلپ کلانژیت صفراوی اولیه – اسکلروزیس سیستمیک و سندروم اورلپ کلانژیت صفراوی اولیه – سندروم شوگرن هم شناسایی می شود.
کد AC-22 : الگوی قطبی / شبه گلژی (Polar/Golgi-like)
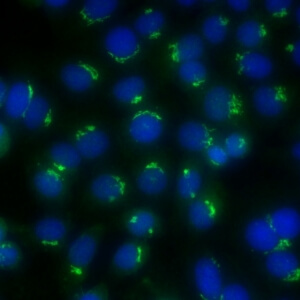
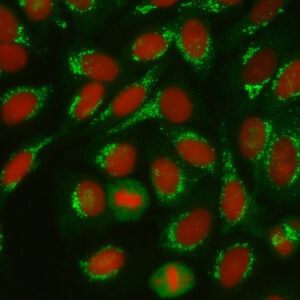
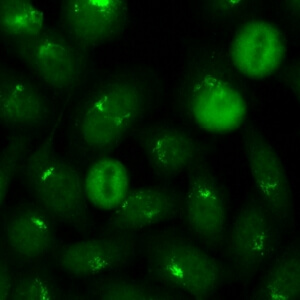
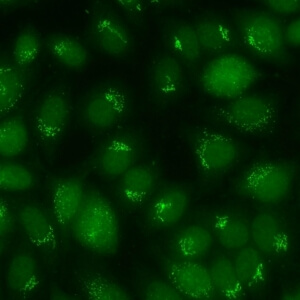
- نام قبلی: –
- توضیحات: رنگ آمیزی لکه دار ناپیوسته یا گرانولار اطراف هسته نواری شکل با توزیع قطبی در سیتوپلاسم. مثال: anti-giantin, anti-golgin-245.
- ارتباط آنتی ژنی: giantin/macrogolgin, golgin-95/GM130, golgin-160, golgin-97, golgin-245
- ارتباط بالینی: در تعداد کمی از بیماران با شرایط مختلف یافت می شود.
کد AC-23 : الگوی میله و حلقه (Rods and rings)
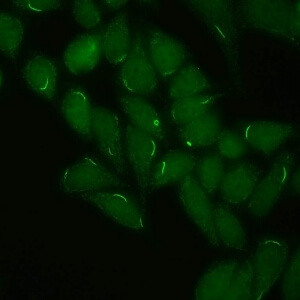
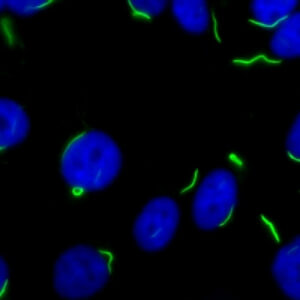
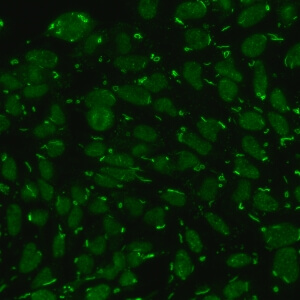
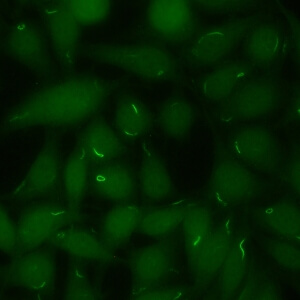
- نام قبلی: –
- توضیحات: ساختارهای میله و حلقه در سیتوپلاسم سلول های اینترفاز. گاها حلقه ها و میله های کوچکتری در هسته دیده شده است.
- ارتباط آنتی ژنی: IMPDH2
- ارتباط بالینی: بیشتر در بیماران مبتلا به هپاتیت C که تحت درمان ترکیبی اینترفرون آلفا پگیله / ریباویرین قرار گرفته اند، یافت می شود.
الگوهای میتوزی
کد AC-24 : الگوی سانتروزوم (Centrosome)
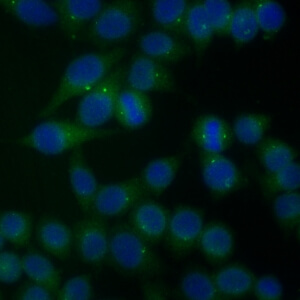
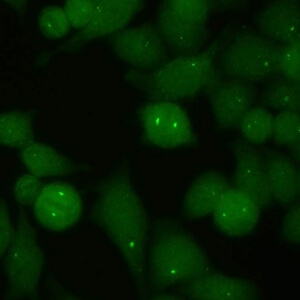
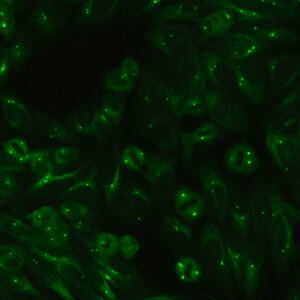
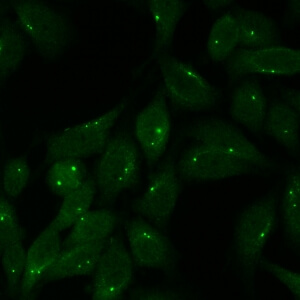
- نام قبلی: سانتریولها
- توضیحات: سانتریول های مجزا (یک تا دو عدد در هر سلول) در سیتوپلاسم و در قطب های دوک میتوزی.
- ساختارهای میله و حلقه در سیتوپلاسم سلول های اینترفاز. گاها حلقه ها و میله های کوچکتری در هسته دیده شده است.
- ارتباط آنتی ژنی: pericentrin, ninein, Cep250, Cep110
- ارتباط بالینی: الگوی AC-24 ارزش اخباری مثبت ناچیزی برای هر نوع بیماری دارد.
کد AC-25 : الگوی فیبرهای دوک (Spindle fibers)
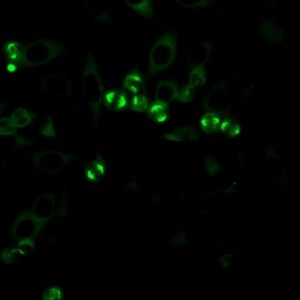
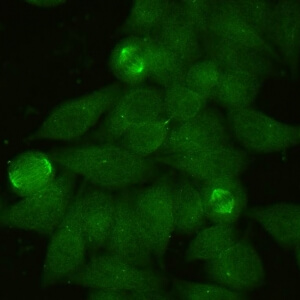
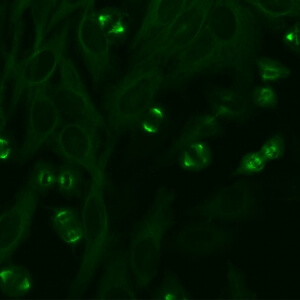
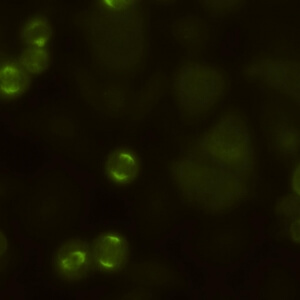
- نام قبلی: –
- توضیحات: فیبرهای دوک بین قطب ها در سلولهای میتوزی رنگ آمیزی می شوند، که با شکل مخروطی قطب های میتوزی همراه است. فیبرهای دوک هم الگوهای شبه دستگاه میتوزی هسته ای و هم الگوهای غیر دستگاه میتوزی را پوشش می دهد. الگوی شبه دستگاه میتوزی هسته ای، با لکه های هسته ای متمایزی مرتبط است.
- ارتباط آنتی ژنی: HsEg5
- ارتباط بالینی: الگوی AC-25 ارزش اخباری مثبت ناچیزی برای هر نوع بیماری دارد.
کد AC-26 : الگوی شبه دستگاه میتوزی هسته ای (nuclear mitotic apparatus-like)
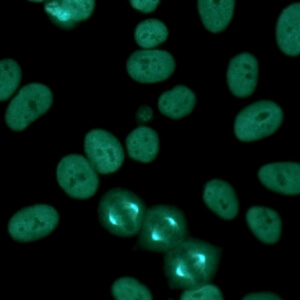
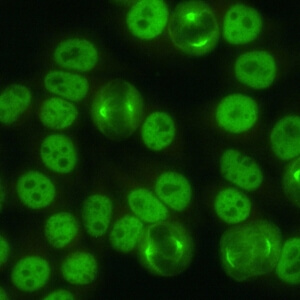
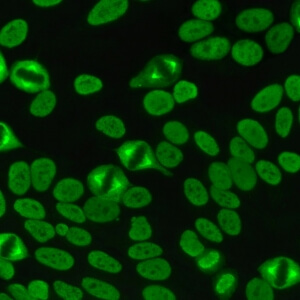
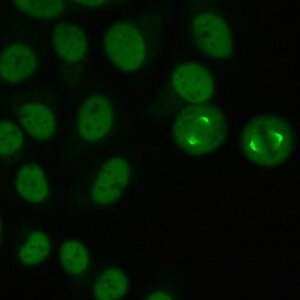
- نام قبلی: MSA-1, centrophilin
- توضیحات: رنگ آمیزی لکه دار هسته ای با فیبرهای دوک
- ارتباط آنتی ژنی: NuMA
- ارتباط بالینی: تقریبا نیمی از بیماران با الگوی AC-26 ، علایم بالینی یکی از بیماری های روماتیسمی اتوایمیون سیستمیک (سندروم شوگرن، لوپوس اریتماتوز سیستمیک، بیماری تمایز نیافته بافت همبند، اسکلروز سیستمیک، یا روماتیسم مفصلی) را دارند. الگوی AC-26 همچنین در افراد مبتلا به بیماری های اتوایمیون اختصاصی ارگان و به میزان کمتری در شرایط غیر اتوایمیون دیده می شود بخصوص زمانی که تیتر بدست آمده پایین است.
کد AC-27 : الگوی پل بین سلولی (Intercellular bridge)




- نام قبلی: stem body, midbody
- توضیحات: رنگ آمیزی پل بین سلولی
- ارتباط آنتی ژنی: –
- ارتباط بالینی: الگوی AC-27 ارزش اخباری مثبت ناچیزی برای هر نوع بیماری دارد.
کد AC-28 : الگوی کروموزومی میتوزی (Mitotic chromosomal)
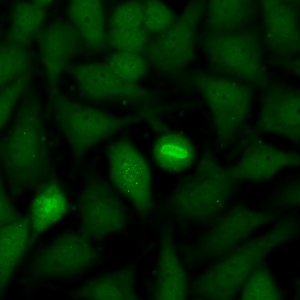
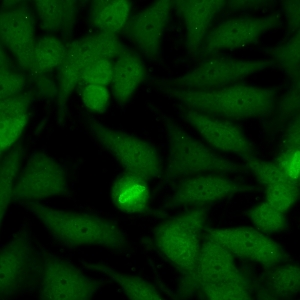
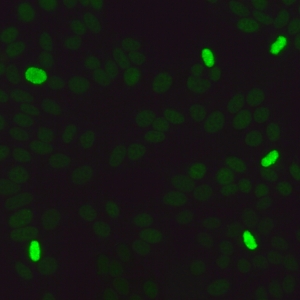
- نام قبلی: پروتئین پوشش کروموزوم، آنتی ژن سلول در حال تقسیم، اتوآنتی ژن کروموزوم میتوزی
- توضیحات: رنگ پذیری سوراخ سوراخ کروموزوم ها در پرومتافاز و متافاز در حالی که سلول های اینترفاز رنگ نمی گیرند.
- ارتباط آنتی ژنی: modified histone H3, MCA-1
- ارتباط بالینی: الگوی AC-28 ارزش اخباری مثبت ناچیزی برای هر نوع بیماری دارد.